Boro
Para acessar o desenho artístico do elemento boro,
clique aqui.
Mapa da chave
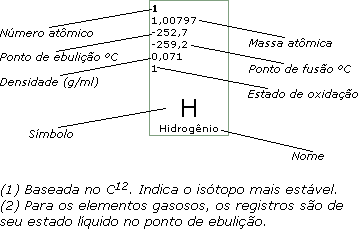
5
10,811
2.550
2.300
2,34
3
B
Boro
|
 |
|
Amostra de Boro. |
Suas propriedades —
grande estabilidade, resistência que o torna imune até ao ácido
clorídrico concentrado em ebulição e índice de dureza próximo ao do
diamante — permitem que o boro tenha múltiplas aplicações, como
antioxidante, anticorrosivo e componente de materiais de
revestimento em geral.
Boro é um elemento
químico semimetálico, de número atômico 5, de símbolo B. Pertencente
ao grupo IIIa
da tabela periódica, junto com o alumínio, o gálio, o índio e o
tálio. Todavia, por suas características especiais de ligação, seu
comportamento assemelha-se mais ao silício. Não encontrado em estado
puro na natureza, aparece sob a forma de ácido bórico e de boratos,
como o bórax, o tincal e a kernita, e integra numerosos compostos
minerais. Em 1702, W. Homberg obteve o ácido bórico a partir do
bórax e denominou-o sal sedativum. Em 1808
Joseph-Louis, Gay-Lussac e Loius-Jacques Thenard, na França, e
Humphry Davy, no Reino Unido, isolaram o boro em forma de pó amorfo
e de cor marrom.
Propriedades físicas
e químicas:
O boro amorfo tem
densidade igual a 2,34. O cristalino, mais puro, é muito duro, tem
brilho quase metálico e densidade igual a 3,3. Funde a 2.300º C e
volatiliza-se um pouco. Em estado puro o não tem muito emprego útil,
mas na forma de ácido bórico e bórax encontra grande aplicação na
indústria. Em eletrônica, é usado como semicondutor, já que sua
condutividade elétrica aumenta com a elevação da temperatura.
O boro se combina tanto
com elementos metálicos quanto não metálicos para formar compostos
covalentes, já que em nenhum caso dá origem a estados catiônicos
(com íons de carga positiva) ou aniônicos (com íons de carga
negativa), o que impede que sejam geradas ligações iônicas.
Ácido bórico:
Conhecem-se vários
ácidos bóricos, todos derivados do anidro bórico, porém o mais
importante é o H3BO3, ácido orto-bórico, que
era obtido por condensação dos vapores vulcânicos que saem, com
temperatura de 90º e 120º C, das fumarolas existentes no denominado
Maremma de Toscana, arrastando quantidades de ácido bórico.
Posteriormente esse ácido passou a ser obtido a partir dos boratos
de cálcio, existentes nos Estados Unidos (na Califórnia) e na
América do Sul.
O ácido bórico é muito
fraco e antigamente era empregado na medicina como anti-séptico e na
conservação de alimentos cosméticos. Essa pratica, todavia, é hoje
proibida ou contra-indicada ou causa das propriedades tóxicas do
ácido. É utilizado também na fabricação de vidros e,
particularmente, nos esmaltes para cobertura de chapas metálicas e
para obtenção de resistência ao calor.
Bórax:
O tetraborato de sódio
(Na2B4O7) existe na natureza sob a
forma de tincal (mineral monoclínico, borato de sódio hidratado),
que contém em média 55% de bórax (tetraborato de sódio decaidratado,
Na2B4O7.10H2O).
Habitualmente, obtém-se o bórax sob a forma de cristais incolores,
ligeiramente solúvel em água fria e mais solúvel em água quente,
sendo suas soluções alcalinas.
O bórax fundido
dissolve alguns óxidos metálicos, formando compostos de coloração
definida; é usado em química analítica nos ensaios de pérola de
bórax. Usam-se grandes quantidades de bórax na fabricação de
esmaltes, vidrados, vidros ópticos; na fabricação de sabão e de
óleos secantes; para enrijecer pavios de vela; como agente de
branqueamento e engomagem em lavanderia; para acetinar papel,
baralhos etc; na fabricação de vernizes, com a caseína; em soldagem,
como fundente; e como anti-séptico.
Os bórax têm grande
importância como aditivo em misturas combustíveis de alta potência.
No Brasil não são conhecidas jazidas de boratos, mas ocorreram
borossilicatos, na formação das turmalinas; porém não são
considerados minérios. Fabrica-se um nitreto de boro conhecido como
borazon, de alta dureza e que é aplicado na fabricação de abrasivos
e peças de grande importância na tecnologia nuclear, como
absorvente.

