Fósforo
Para acessar o desenho artístico do elemento fósforo,
clique aqui.
Mapa da chave
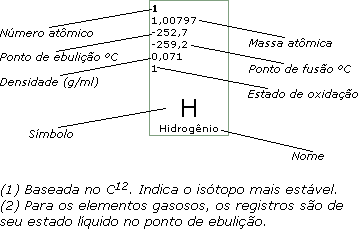
15
30,9738
280 b
55,2
b
1,82
+3,5,4
P
Fósforo
|
 |
|
Fluorapatita, fonte de
fósforo. |
Numa das tentativas de
encontrar a pedra filosofal, o alquimista alemão Hennig Brand isolou
pela primeira vez, em 1669, fósforo elementar a partir de resíduos
de urina evaporada. O brilho emitido pela substância no escuro está
na origem de sua denominação: do grego phós, “luz”, e
phóros, “transportador”.
Fósforo é um elemento
químico não-metálico, de símbolo P e número atômico 15, incluído no
grupo Va
do sistema periódico, que corresponde ao dos nitrogenóides, muito
inflamável, luminoso na obscuridade. Encontra-se na natureza em
combinações de fosfatos e outros sais. Como componente orgânico,
encontra-se nos nos organismos vivos sob as formas de fosfatos de
cálcio nos ossos e nos dentes (metabolismo fosfocálcio), de ésteres
ortofosfóricos (associado a ossos, a ácidos aminados, a bases), de
ésteres difosfóricos (adenosina difosfórica ou A.D.P., que
desempenham um papel importante na reserva genética), de nucleotídeo
no ácido desoxirribonucléico (A.D.N.), faz parte da urina, do sangue
e de outros humores ou líquidos corporais.
Propriedades físicas
e químicas:
O estado
fundamental do átomo de fósforo apresenta uma estrutura de elétrons
representada na configuração 1s22s22p63s23p3.
Isso implica uma camada externa de cinco elétrons sobre os quais o
núcleo exerce intensa atração. Conseqüentemente, as ligações do
átomo de fósforo com outros átomos próximos mostram uma natureza
covalente, isto é, compartilham elétrons em suas uniões.
O fósforo apresenta dez
variedades alotrópicas — manifestações diversas de composições
químicas análogas — das quais as três mais importantes são o fósforo
branco, o vermelho e o negro. O primeiro, fortemente tóxico,
apresenta-se sob duas formas: alfa, de estrutura cristalina cúbica
(embora exista uma variedade hexagonal) e estável à temperatura
ambiente; e beta, de estrutura hexagonal e estável apenas a
temperaturas inferiores a -78º C. De molécula tetratômica (P4),
é instável, muito reativo e, em contato com o ar, se inflama
espontaneamente e experimenta oxidação lenta, que ocasiona formação
de anidrido fosfórico P4O10 e emissão de
luminosidade, fenômeno conhecido como fosforescência.
Exposto à luz, o
fósforo branco passa à forma vermelha, com estrutura em camadas
alternadas entre as quais se dispõem outras moléculas P4
do estado branco. O fósforo vermelho não é venenoso nem
fosforescente e apresenta uma reatividade muito inferior. Nesse
estado alotrópico é utilizado para sua aplicação mais comum: a
fabricação de palitos de fósforo. Mais raro que as variedades
anteriores, o fósforo negro é o mais estável do ponto de vista
termodinâmico. Sua estrutura consiste de camadas em ziguezigue de
átomos de fósforo.
Estado natural e
obtenção:
O fósforo não se
encontra livre na natureza em nenhuma de suas variedades mas, em
combinações como os fosfatos, constitui 0,12% da composição da
crosta terrestre e, em ordem quantitativa, é o duodécimo elemento
químico na Terra. As matérias-primas a partir das quais se extrai o
fósforo são fundamentalmente os fosfatos de metais alcalino-terrosos
encontrados em depósitos de rochas de fosfato, como a clorapatita,
Ca5(PO4)3Cl, a fluorapatita,
Ca5(PO4)3F ou a vivianita, Fe3(PO4)2.8H2O.
Quanto a seu papel
biológico, o fósforo encontra-se nos organismos vivos em combinação
oxigenada, geralmente como anidrido P2O5, como
suporte de reações metabólicas. A presença desse elemento em níveis
adequados é especialmente importante nos ossos, em que atua como
suporte dos compostos de cálcio. Especial interesse apresentam as
fosfatases, enzimas contidas na maior parte das secreções e células
do organismo humano, que intervêm em processos fisiológicos das mais
diversas índoles, como a precipitação de fosfato de cálcio no tecido
ósseo, a síntese de proteínas nos tecidos e a absorção de fosfatos
no intestino.
Para a bioquímica, o
fósforo também constitui elemento básico, já que faz parte da
composição do ATP, trifosfato de adenosina, e do ADP, difosfato de
adenosina, nucleotídeos presentes nos tecidos, que desempenham
função essencial tanto no metabolismo molecular como na regulação
entre absorção e liberação energéticas.
Aplicações:
Tanto o fósforo
elementar como suas combinações apresentam amplo espectro de
aplicações. Por ser essencial aos processos vitais, esse elemento é
o constituinte básico, por exemplo, de muitos preparados
farmacêuticos utilizados como reconstituintes e fixadores de cálcio.
Uma de suas primeiras e mais generalizadas aplicações foi a
fabricação dos palitos de fósforo, chamados fósforos de segurança. O
fósforo branco inicialmente empregado para esse fim foi
progressivamente substituído, em razão de sua toxicidade, por um de
seus compostos, o trissulfureto fosfórico, P4S3.
É precisamente o efeito
venenoso do fósforo branco que o tornou útil como substância ativa
de diversos inseticidas e raticidas, mas para esse uso também foi
substituído para evitar riscos de envenenamento dos aplicadores. Os
compostos fosforados se empregam industrialmente como aditivos da
gasolina e dos plásticos, na fabricação de detergentes e, em
metalurgia, como protetores. Boa parte do fósforo usado na indústria
é obtida em forma de fosfatos, extraídos de diferentes minerais e
utilizados como fertilizantes.
As reservas brasileiras
de fosfatos são dos seguintes tipos: jazidas de apatita ligadas a
rochas graníticas; jazidas de apatita ligadas a rochas eruptivas;
jazidas de fosfatos sedimentares em camadas de origem marinha;
jazidas de aluminofosfatos de origem organomineral e depósitos de
guano. Exploram-se as do segundo e do terceiro tipos. A principal
reserva é a de Araxá, em Minas Gerais, com cem milhões de toneladas
de apatita; seguem-se as de Olinda, em Pernambuco, e Jacupiranga, em
São Paulo.

