Nitrogênio
Para acessar o desenho artístico do elemento nitrogênio,
clique aqui.
Mapa da chave
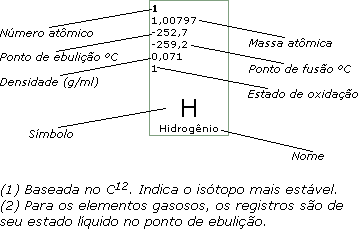
7
14,0067
-195,8
-210
-081
±3,5,4,2
N
Nitrogênio
|
 |
|
Nitrato de sódio,
fonte de nitrogênio. |
Os animais obtêm
nitrogênio para a elaboração das proteínas essenciais à vida a
partir dos vegetais ou de outras proteínas animais presentes nos
alimentos, enquanto as plantas sintetizam suas proteínas a partir de
compostos nitrogenados inorgânicos que retiram do solo e, até certo
ponto, do nitrogênio livre na atmosfera.
O nitrogênio é um
ametal do grupo Va
da tabela periódica, de símbolo químico N. É o elemento mais
abundante da atmosfera terrestre e está presente em todos os seres
vivos. Apresenta dois isótopos estáveis e forma o gás nitrogênio (N2),
insípido, inodoro e incolor. Por sua alta energia de ligação, o
nitrogênio molecular não reage facilmente com outras substâncias e,
sob condições normais, é relativamente inerte à maioria dos
reagentes.
Atribui-se a Daniel
Rutherford a descoberta do nitrogênio em 1772, porque o cientista
foi o primeiro a publicar suas descobertas, mas, na Grã-Bretanha, os
químicos Joseph Priestley e Henry Cavendish e, na Suécia, Carl
Wilhelm Scheele também descobriram o elemento na mesma época.
Lavoisier, o primeiro a reconhecer que se tratava de um elemento
químico independente e a identificá-lo em certos compostos minerais,
deu-lhe o nome de azoto (do grego a, “sem”, e zoe, “vida”) em razão
de sua incapacidade para manter a vida e alimentar a combustão. O
nome nitrogênio foi criado em 1790, por Jean-Antoine Chaptal, após a
descoberta de sua relação com o ácido nítrico.
Ocorrência:
Entre os elementos, o
nitrogênio é o sexto em abundância no universo. Constitui cerca de
78% do volume atmosférico. Encontra-se nitrogênio livre em muitos
meteoritos, nos gases de vulcões, minas e em algumas fontes
minerais, no Sol, em estrelas e nebulosas. Em combinação com outros
elementos, ocorre nas proteínas; no salitre do Chile (nitrato de
sódio, NaNO3),
muito usado como fertilizante; na atmosfera, na chuva, no solo e no
guano (adubo natural formado a partir da decomposição dos
excrementos e cadáveres de aves marinhas), sob a forma de amônia e
sais de amônio; e na água do mar, como íons de amônio (NH4+),
nitrito (NO2¯) e nitrato (NO3¯).
Obtenção:
A produção comercial de
nitrogênio se realiza por destilação fracionada do ar líquido,
mediante a qual se elimina o oxigênio da mistura. Esse processo é
possível graças à grande diferença entre os pontos de ebulição de
ambos os elementos. Em escala reduzida, o nitrogênio puro é obtido
em laboratório por inúmeras reações de oxidação da amônia e seus
derivados ou por redução de compostos oxigenados do nitrogênio.
Entre os mais comuns, citam-se a decomposição térmica do dicromato
de amônio e do nitrito de amônio.
Aplicações:
Quase inerte, o
nitrogênio gasoso se emprega na indústria química como solvente,
como protetor de outros produtos contra eventuais riscos de oxidação
ou deterioração ou como inibidor de possíveis combustões e
explosões.
Na indústria
alimentícia, é utilizado em estado gasoso para prevenir a oxidação e
o aparecimento de mofo ou insetos. Em estado líquido, é usado nos
sistemas de refrigeração e como congelante seco. O baixo ponto de
ebulição do nitrogênio recomenda seu uso como agente criogênico para
a maioria das substâncias químicas e proporciona valiosos dados
sobre o comportamento da matéria a baixas temperaturas.
As indústrias
metalúrgica e elétrica recorrem ao nitrogênio para prevenir a
oxidação. O caráter estável e a baixa reatividade do nitrogênio
gasoso recomendam seu emprego no fabrico de espumas de borracha e
plásticos, na obtenção de aerossóis e na pressurização de
propulsores líquidos para jatos de reação. Na medicina, a substância
também é largamente aproveitada, por seu rápido congelamento, como
conservante de sangue, sêmen, tecidos, bactérias etc.
Ciclo do nitrogênio:
O nitrogênio é um dos
elementos indispensáveis à vida. Incapazes de assimilar nitrogênio
livre ou proveniente de compostos inorgânicos, os animais retiram-no
de outros animais ou de vegetais, estes sim capazes de assimilar
compostos nitrogenados inorgânicos extraídos do solo. O consumo do
nitrogênio do solo se compensa pela adição de fertilizantes ou por
processos naturais: o nitrogênio do ar pode ser fixado por meio de
descarga elétrica na atmosfera; forma-se ácido nítrico, que é
conduzido pela chuva ao solo, onde forma nitratos.
Outra forma de fixação
do nitrogênio pode ser observada em dois tipos de bactérias: (1) as
do gênero Rhizobium, que se alojam nos nódulos das raízes das
leguminosas e sintetizam, com o nitrogênio do ar, compostos
orgânicos nitrogenados utilizados pela planta na síntese das
proteínas; (2) as saprófitas (Azotobacter e Clostridium), que
combinam o nitrogênio atmosférico com carboidratos. Na decomposição
de restos animais e vegetais, o nitrogênio dos mesmos se transforma
principalmente em amônia (amonificação), por ação das bactérias
amonificantes. A amônia formada pode ser atacada pelas bactérias
nitrificantes, para produzir nitrito. Este, sob a ação das
Nitrobacter, passa a nitrato. As bactérias desnitrificantes podem
reduzir nitratos novamente a nitrogênio, que retorna à atmosfera.
Fixação do
nitrogênio:
Como as jazidas de
salitre do Chile têm capacidade limitada, tornou-se necessário
utilizar o nitrogênio atmosférico, que é praticamente inesgotável.
Esse aproveitamento exige a fixação do nitrogênio, isto é, sua
combinação com outros elementos.
Método da descarga
elétrica:
A passagem de uma
descarga elétrica através do ar provoca a combinação do nitrogênio
com o oxigênio para formar NO, que passa depois a NO2. O
NO2 dissolvido em água produz ácido nítrico. Em água de
cal produz nitrato de cálcio.
Método
da cianamida cálcica:
Submetido a temperatura
elevada, o nitrogênio produz, com carbureto de cálcio, a cianamida
cálcica: CaC2 + N2
®
CaCN2 + C. O carbureto de cálcio se obtém por aquecimento
da cal em forno elétrico. O nitrogênio, que deve ter a pureza de
pelo menos 99,8%, é obtido do ar líquido. A hidrólise da cianamida
produz amoníaco: CaCN2 + 3H2O
®
2NH3 + CaCO3.
Método
de cianeto de sódio:
Quando se passa
nitrogênio sobre uma mistura de carbono e carbonato de sódio
aquecida ao rubro, obtém-se cianeto de sódio, segundo a equação: Na2CO3
+ 4C + N2
®
2NaCN + 3CO. O ferro age como catalisador. As tentativas de
aplicação industrial não obtiveram sucesso.
Método da síntese direta do amoníaco:
O nitrogênio combina-se
com o hidrogênio, no principal processo de obtenção de NH3,
segundo a reação: 2N2 + 3H2
®
2NH3.
Compostos
nitrogenados:
O amoníaco (NH3),
conhecido pelo odor característico e irritante, é um gás incolor
resultante da combinação direta do nitrogênio com o hidrogênio sob
temperatura elevada, comercializado normalmente como solução aquosa.
Se emprega como fertilizante e como fonte de vários compostos
nitrogenados comercialmente importantes. O principal método
comercial de síntese de amoníaco é o processo de Haber-Bosch.
Outro composto
nitrogenado, o ácido nítrico (HNO3) é um ácido forte,
também de larga aplicação científica e industrial. O caráter
oxidante, comparável ao do ácido sulfúrico, justifica seu uso nos
processos de oxidação-redução de metais para produzir sais
(nitratos). Prata, mercúrio e cobre reagem com o ácido concentrado
para produzir NO2 e com ácido diluído para dar origem a
NO. Ouro, platina, irídio, ródio, lantânio e titânio não são
atacados. Misturado ao ácido clorídrico na proporção de um para
três, é chamado água-régia, pois ataca os metais nobres, inclusive o
ouro.
De menor ação
corrosiva, o ácido nitroso não existe em estado puro, mas só em
solução resultante da decomposição à temperatura ambiente em óxido,
ácido nítrico e água. Os nitritos e nitratos, sais respectivamente
derivados dos ácidos nitroso e nítrico, são habitualmente usados em
fertilizantes.
Os óxidos nitroso e
nítrico são substâncias de alta reatividade, enquanto o dióxido de
nitrogênio apresenta maior estabilidade interna. Juntamente com o
óxido nítrico, o dióxido de nitrogênio se encontra em pequena
proporção na atmosfera. Oriundo de resíduos industriais da indústria
química, é um poderoso agente de contaminação ambiental.
Propriedades físicas e químicas do
nitrogênio:
|
|
Número atômico: |
7 |
|
Peso atômico: |
14,0067 |
|
Ponto de
fusão: |
-210º C |
|
Ponto de
ebulição: |
-195,8º C |
|
Densidade
(20º): |
1,250 g/l |
|
Estados de
oxidação: |
-3, +3, +5 |
|
Configuração
eletrônica: |
1s22s22p3 |

