Oxigênio
Para acessar o desenho artístico do elemento oxigênio,
clique aqui.
Mapa da chave
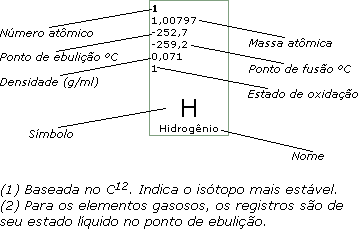
8
15,9944
-183
-218,8
1,14
2
O
Oxigênio
|
 |
|
Joseph Priestley,
descobridor do oxigênio. |
Durante muito tempo o
ar foi considerado um elemento químico e só no final do século XVIII
reconheceu-se que ele era na verdade uma mistura, cujo constituinte
ativo é atualmente chamado oxigênio.
O oxigênio, elemento
químico de símbolo O, pertencente ao grupo dos calcogênios (VIa),
foi descoberto por Priestley em 1722, por calcinação do nitrato de
potássio. A partir de 1775, Lavoisier estabeleceu suas propriedades,
mostrou que existia no ar e na água, e indicou seu papel fundamental
nas combustões e na respiração. Coube ao químico francês Antoine
Lavoiser mostrar que a combustão, a calcinação dos metais e a
respiração são fenômenos relacionados entre si, pois são todos
processos de combinação com o oxigênio.
Propriedades físicas
e químicas:
O oxigênio natural é um
gás incolor e inodoro, com densidade 1,105, que só liquefaz a -138º
C, consiste numa mistura de três isótopos estáveis: o oxigênio 16
(99,758%), o oxigênio 17 (0,37%) e o oxigênio 18 (0,204%). Pouco
solúvel em água, forma bolhas que se desprendem facilmente por
simples agitação. À temperatura ambiente, a molécula de oxigênio é
relativamente inerte, mas na presença de substâncias catalisadoras
ou ao ser aquecida, reage com a maioria dos elementos para formar
vários compostos.
Na baixa atmosfera e à
temperatura ambiente, o oxigênio está presente na principalmente na
forma de moléculas diatômicas (O2) que constituem um gás
incolor, inodoro e insípido, essencial para os organismos vivos.
Apresenta densidade levemente superior à do ar e seus átomos são
respectivamente pequenos, pois possuem oito elétrons (partículas
elementares de carga negativa). Muito eletronegativo, une-se aos
ametais (com exceção dos halogênios) e aos ametais, salvo o ouro e a
platina. Essas combinações, que em geral desprendem calor, são
chamadas “combustões” e podem ser vivas ou lentas. É o elemento mais
abundante do globo terrestre. Constitui aproximadamente um quinto do
ar, oito nonos do peso da água; figura na maioria dos constituintes
do solo (silicatos, carbonatos) e das substância orgânicas. Sua
combustão fornece vapor de água e gás carbônico, mas, se o oxigênio
se encontra em quantidade insuficiente, o hidrogênio queima antes do
carbono, do qual uma parte torna a chama brilhante e aparece sob
forma de negro-de-fumo.
Descoberta e métodos
de obtenção:
Embora o químico sueco
Carl Wihelm Scheele tenha conseguido preparar uma amostra de
oxigênio em 1772, atribui-se tradicionalmente seu descobrimento ao
britânico Joseph Priestley, que sintetizou o gás em 1774 e publicou
antes de Scheele o resultado de suas experiências. O trabalho de
Priestley, aperfeiçoado depois por Lavoisieir (que criou o nome
oxigênio), se baseava no aquecimento de óxido de mercúrio, que
produzia um gás puro, perfeitamente respirável, consumido por
completo em novas combustões.
Esse método, também
aplicado aos óxidos de prata e de bário e a certa variedade de sais,
produz oxigênio de grandeza pura, ainda que em pequenas quantidades.
Outra fonte comum de síntese do oxigênio em laboratório é a
decomposição da água oxigenada. Na indústria, são mais utilizadas a
eletrólise da água, que resulta na separação de seus dois elementos
constituintes, hidrogênio e oxigênio; e a destilação fracionada do
ar liquido. O primeiro processo consiste em submeter à ação de
corrente elétrica uma cuba eletrolítica cheia de água, à grave; qual
se adicionou uma substância condutora, como o ácido sulfúrico ou a
soda cáustica. A destilação fracionada do ar líquido, processo de
maior rentabilidade econômica para aplicação em grande escala, se
baseia na diferença existente entre os pontos de ebulição do
nitrogênio e do oxigênio, componentes mais abundantes na mistura.
Variedades
alotrópicas:
O oxigênio apresentasse
habitualmente na forma de moléculas diatômicas, mas se altera sob a
ação de fortes descargas elétricas ou na presença de substâncias
ionizadas que tenham perdido parte de sua carga eletrônica ou
capturado partículas do ambiente. Produz-se dessa maneira uma
variedade alotrópica chamada ozônio, de molécula O3. Essa
substância, empregada industrialmente como descolorante,
esterilizador de líquidos e depurador de ambientes, está presente
nas altas camadas da atmosfera. Desempenha um papel fundamental na
manutenção da vida sobre a Terra ao proteger o planeta da radiação
ultravioleta do Sol.
Compostos
oxigenados:
A combinação do
oxigênio com outros elementos forma óxidos, cuja reação com a água
produz oxiácidos e bases. A combinação dos quais existem numerosas
famílias e variedades, presentes na natureza na maioria dos
fenômenos geológicos. Inúmeras substâncias orgânicas, como álcoois,
ésteres, aldeídos, cetonas, ácidos carboxílicos e ésteres, também
possuem átomos de oxigênio em sua estrutura.
Processos de
oxidação:
A reação espontânea de
qualquer substância com o oxigênio é denominada oxidação (termo que
também designa qualquer processo na qual uma substância perde
elétrons). Quando a reação é imediata e produz calor e luz, chama-se
combustão. São exemplos de processos de oxidação a corrosão do ferro
e a putefração da madeira, que formam óxidos de ferro e de carbono,
respectivamente. A queima da madeira gera os mesmos produtos de sua
putefração: dióxido de carbono e água. Os fenômenos de combustão
podem ser espontâneos e, em substâncias como o carvão betuminoso,
provocar incêndios em virtude da reação instantânea entre oxigênio,
carbono e hidrogênio.
Aplicações:
São inúmeras as
aplicações do oxigênio na indústria. Vários tipos de maçaricos —
como os oxiacetilênicos, produtores de feixes de grande conteúdo
energético, que soldam ou seccionam metais; os oxídricos, que
fabricam delicados dispositivos de quartzo e platina; e os de gás,
úteis no tratamento de vidros — permitem a realização de tarefas
específicas de soldura nas indústrias de base e de construção. O
oxigênio líquido, misturado a outros combustíveis é utilizado como
explosivo.
Certos trabalhos que
exigem a permanência do homem em ambientes hostis demandam o
transporte do oxigênio necessário à respiração. Submarinos, aviões,
naves espaciais, prospecções minerais e geológicas a grandes
profundidades são abastecidos com tanques e bombas de oxigênio
quando não é possível empregar dispositivos de injeção de ar a
partir do exterior. Nos centros médicos é comum a administração de
oxigênio a pacientes asmáticos ou com problemas pulmonares. Também é
aconselhável em processos de envenenamento, nos quais é preciso
acelerar os mecanismos de oxidação do sangue.
Propriedades físicas e químicas do
oxigênio:
|
|
Número atômico: |
8 |
|
Peso atômico: |
15,9994 |
|
Ponto de
fusão: |
-218,4º C |
|
Ponto de
ebulição: |
-183,0º C |
|
Densidade: |
1,429g/l |
|
Estados de
oxidação: |
-2 |
|
Configuração
eletrônica: |
1s22s22p4 |

